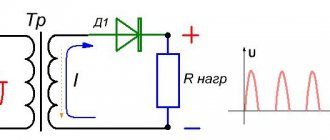
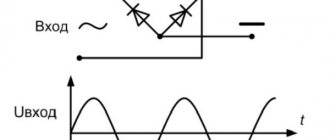
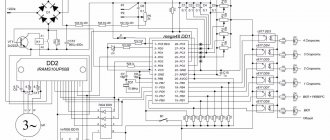
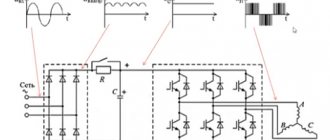
Свинцово кислотный аккумулятор – источник тока, питающий стартер при запуске двигателя. АКБ является основным источником энергии. Среди преимуществ данного типа аккумуляторных батарей – увеличенный срок службы, составляющий более 500 циклов, высокая удельная мощность, стоимость. Помимо транспортных средств, свинцовые аккумуляторы встречаются в резервных и аварийных источниках энергии стационарного и мобильного типа.
Принцип работы свинцово-кислотного аккумулятора заключается в преобразовании химической и электрической энергий.
Устройство
Конструктивно кислотный аккумулятор состоит из следующих элементов:
- Корпус. Представляет собой моноблок. В него помещаются аккумуляторы. Изготовлен из изолирующего материала, стойкого к кислоте. Как правило, это пропилен.
- Электрод (решётка, покрытая пастой из свинцово-оксидного порошка). Положительные электроды покрыты диоксидом свинца. Отрицательно заряжённые решётки покрыты массой губчатого свинца. Для того чтобы увеличить антикоррозийную стойкость электродов, ряд производителей в свинцово-кальциевый сплав добавляет пассиваторы
- Сепаратор-конверт. Устанавливается для изоляции решёток, пластин противоположной полярности в батарейных элементах. В случае соприкосновения пластин разной полярности произойдёт короткое замыкание. Главная сложность при изготовлении сепараторов: их материал должен уберечь от такого замыкания, при этом ток должен беспрепятственно проходить через электролит. Компромиссное решение и достойный вариант материала – микропористая пластмасса. Большинство свинцово-кислотных батарей используют активное вещество электродов из свинцово-кальциевого сплава. У них минимальный уровень саморазряда.
- Шина
- Крышка
- Выходное отверстие.
- Клеммы. Обеспечивают непосредственную связь батареи со стартером, генератором, позволяют быстро монтировать или демонтировать батарею.
- Индикаторы плотности электролита и заряженности батареи.
Каждая современная батарея состоит из шести кислотных аккумуляторов. Используется последовательное соединение. Шесть 2-х вольтовых элементов обеспечивают на выходе 12 вольт.
Типы свинцово-кислотных аккумуляторов
Квалифицировать АКБ можно по двум признакам по функциональному назначению и установленному электролиту. По функциональному назначению устройства бывают двух типов:
- Стартерные.Обеспечивают запуск двигателя автомобиля, подают ток на стартер. Требуют обслуживания и вентиляции.
- Тяговые. Устройства для цикличных режимов. Используются в ситуациях, когда нужно обеспечить механизмы непрерывной энергией (питания в постоянном режиме). Чаще всего устанавливаются на электрокарах, тягачах, погрузчиках.
Что касается второго классификационного признака — тип электролита, то он может быть абсорбируемым, жидким, гелеообразным. В большинстве случаев мы имеем дело с жидкой средой. Электроды находятся в электролите из раствора серной кислоты.
Плотность электролита в зависимости от степени заряженности постоянно изменяется. Чем заряжённость элемента ниже, тем ниже плотность электролита. При полном заряде плотность достигает 1.29 г/см3.
У ряда же современных АКБ электролит удерживается в специальном микропористом материале. В этом случае речь и идёт об абсорбируемом электролите. Объём электролита, заливаемый в АКБ добавляются в том объёме, который может впитать микропористый материал. Лучшее поглощение кислоты влечет за собой повышение эффективности активной массы. Это очень ценно, если АКБ работает на систему рекуперативного торможения или систему стоп-старта. Но из-за высокой стоимости батарей такого типа массового перехода на них пока нет. Большинство использует традиционные свинцово-кислотные батареи.
Наиболее хорошо известны решения, которые ориентированы на абсорбированные электролиты. Это батареи, изготовленные по технологии AGM. Обслуживание свинцово-кислотных аккумуляторов такого типа не требуется. Для установки не нужно заботиться о том, чтобы помещение было вентилируемым. Работа не требует обслуживания. При этом в режиме подзарядки (буферном режиме) батареи способны служить 12-18 лет, в цикличном режиме — меньше.
Как выбрать аккумулятор
Выбор моделей, представленных в магазинах, велик. Чтобы купить свинцово-кислотный АКБ, рекомендуется обращать внимание на следующие нюансы:
- Размер. При подборе аккумулятора важен размер, который должен соответствует нише в моторном отсеке.
- Полярность. Расположение клемм нового АКБ и старого должны совпадать.
- Бренд. Эксперты рекомендуют выбрать аккумулятор для автомобиля известного производителя, что гарантирует качество продукции в течение заявленного срока.
- Тип. Обслуживаемый или необслуживаемый. Во втором случае батарея не требует дополнительного ухода, но при глубоком переразряде её нельзя будет регенерировать.
- Заявленный ток. Чем выше параметр, тем ниже внутренне сопротивление, тем качественней модель.
Свинцово-кислотная батарея из-за потребительских характеристик – практически безальтернативный вариант для установки в автомобиле. При этом производители предлагают сотни вариантов, отличающихся по цене, техническим характеристикам, ориентированных на разных клиентов.
Принцип работы аккумуляторной батареи
Как работает аккумуляторная батарея автомобиля?
- При заряде электрическая энергия преобразуется в химическую энергию.
- При разряде химическая энергия преобразуется в электрическую.
- Работа аккумулятора циклична.
Таким образом, принцип действия базируется на преобразовании электрической энергии в химическую (этот процесс происходит при заряде) и химической энергии в электрическую (напротив, при разряде). И затем этот процесс повторяется.
На работу влияет окружающая температура. Если температура воздуха возрастает, увеличивается отдаваемая аккумулятором мощность. Казалось бы, проблема эффективности решена. Но не всё так просто, одновременно существенно увеличивается склонность батареи к саморозряду и к корродированию.
Понижение температуры в свою очередь, приводит к уменьшению разрядной емкости, а также уменьшению плотности электролита.
Конструкция
Кислотные батареи уже более ста лет не меняются по своему основному внутреннему устройству.
В конструкцию аккумуляторных батарей входят:
- Электроды – в виде плоских решеток из свинца, в ячейки запрессован порошок диоксид свинца (PbO2) на аноде, порошок металлического свинца (Pb) — на катоде.
- Сепаратор — пористый диэлектрик, разделяет между собой электроды, препятствуя замыканию.
- Электролит — разбавленная водой (дистиллированной) серная кислота H2SO4, в нее помещены электроды и сепаратор. Максимальная электропроводность достигается при температуре 20оС, концентрации серной кислоты – 35 %, что означает плотность электролита 1,26 г/см³. Внутренне сопротивление при этом минимально, потери внутри устройства существенно малы. В местах с низкотемпературным климатом возможно повышение плотности раствора до 1,29 г/см³ – 1,31 г/см³. Увеличение концентрации кислотного раствора препятствует замерзанию электролита, образованию льда внутри корпуса, который может повредить электроды и разорвать аккумулятор.
Преимущества и недостатки
Популярность кислотно-свинцовых устройств легко объяснить множеством факторов.
- Низкой себестоимостью и, соответственно, доступной ценой.
- Надёжностью.
- Малой саморазрядностью.
- Простотой в обслуживании (не нужно доливать электролит),а для некоторых моделей, как, например, решений по технологии AGM, и вовсе отсутствие необходимости в сервисе.
Тем не менее, человечество постоянно ищет альтернативу, в ряде случаев использует щелощные устройства. Почему? Это связано с тем, что у кислотного оборудования есть и недостатки:
- Трудности с организацией хранения. Хранение возможно исключительно в заряжённом виде.
- Плохая переносимость переразрядов. Правила эксплуатации ограничивают количество циклов заряда- разряда.
- Вред для окружающей среды (выделение испарений).
- Высокие риски перегрева при неправильной зарядке.
- Нестабильная работа в условиях низких температур. Иногда из-за этого возникают проблемы с запуском мотора в зимнее время.
- Слабые возможности на протяжении длительного времени в тяговом режиме эксплуатации выдавать электрический ток.
Аккумуляторы GEL и AGM
Примеры аккумуляторов AGM
Для многих сфер требуются батареи, которые безопасны в эксплуатации, полностью герметичны и не пропускают кислоту. Их называют батареями VRLA (свинцово-кислотные батареи с регулируемым клапаном), иногда также называемые SLA (герметичные свинцово-кислотные батареи). Основой здесь является не только использование герметичных клапанов, но и улавливание электролита в банках.
Известны два типа батарей VRLA – более популярные AGM и гораздо менее распространенные гелевые (GEL).
AGM означает «Абсорбированный стеклянный мат». В ячейках между пластинами находится стекловата (мат), в которой задерживается электролит. С другой стороны, в гелевых батареях электролит находится в форме геля благодаря добавке кремнезема.
Обычный пользователь не заметит разницы между AGM и гелевыми на глаз, потому что их конструкция и корпус могут быть одинаковыми. Часто метка AGM на аккумуляторе отсутствует; надпись GEL не всегда бывает на геле. Такие герметичные батареи ошибочно называют «гелевыми», хотя наиболее распространенными являются батареи типа AGM.
Различия между AGM и гелевыми батареями в основном состоят в долговечности и рекомендуемых условиях зарядки и разрядки. Как правило, большинство GEL не могут работать при высоких токах, поэтому, например, для ИБП обычно используются аккумуляторы AGM. С другой стороны, GEL обычно служат дольше, но только в более мягких условиях эксплуатации. Правда есть гелевые аккумуляторы для тяжелых циклических работ и глубокого разряда.
Следует подчеркнуть, что преимуществом AGM и гелевых аккумуляторов являются, с одной стороны, их герметичность и необслуживаемость, а с другой – они требуют тщательно подобранных условий зарядки. Хотя у них есть клапаны, но они будут работать только в случае выхода из строя, когда происходит перезарядка и сильное газообразование.
У них во время правильной зарядки выделяется определенное количество газов, давление увеличивается, но благодаря присутствию катализатора происходит рекомбинация, то есть повторное преобразование водорода и кислорода в воду. Клапаны закрыты и открываются только при особо большом увеличении давления, когда происходит сильное газообразование из-за перезарядки.
Внимание: даже однократная сильная перезарядка очень вредна и может необратимо снизить емкость AGM и гелевых аккумуляторов. В то время как в случае старых классических открытых батарей газообразование было допустимо, в AGM и гелевых батареях выделение газа запрещено.
Чрезмерный разряд тоже очень вреден, особенно в батареях AGM. Существует несколько неблагоприятных явлений, включая так называемую сульфатацию, то есть образование непроводящего слоя кристаллов сульфата свинца внутри батареи. Даже однократный разряд до нуля может вызвать серьезную необратимую потерю емкости и такую разряженную батарею следует как можно скорее перезарядить.
Поэтому важно как не перезаряжать, так и не разряжать аккумулятор. На самом деле это просто. Чтобы предотвратить перезарядку, достаточно ограничить зарядное напряжение до безопасного значения. Чтобы предотвратить чрезмерную разрядку, стоит использовать схему сигнализации падения напряжения и добавить схему автоматического отключения.
Зависимость времени автономной работы от глубины разряда
Автомобильный аккумулятор заданной емкости однозначно дешевле «неавтомобильного» такой же емкости. В основном это связано с тем, что автомобильный АКБ рассчитан на работу в относительно мягких условиях.
Хотя перепады температур при его использовании большие, от -20 ° C до более + 40 ° C, в автомобиле он постоянно заряжается генератором и регулятором, затем напряжение держится на уровне 14,4 В. Конечно присутствует высокий ток в течение нескольких секунд во время запуска и небольшой ток во время простоя.
Соответственно, автомобильные аккумуляторы имеют относительно простую конструкцию и не подходят для интенсивной езды на велосипеде, когда они почти полностью разряжены после зарядки. При интенсивных циклах (зарядка / полная разрядка) они просто будут иметь очень короткий срок службы и потеряют емкость уже после небольшого количества циклов.
Для тяжелых циклических работ, например, в электропогрузчиках или тележках, производятся так называемые тяговые батареи, которые более мощные, но и более дорогие.
Надёжность сильно зависит от глубины разряда. Если хотим увеличить срок службы, то должны получить аккумулятор большей емкости, чем требуется, и никогда не разряжать его полностью.
Есть много типов «неавтоматических» кислотных аккумуляторов. Все они подходят для мягких условий буферизации. Но не все из них подходят для тяжелой циклической работы – здесь следует использовать предназначенные специально для такой работы «усиленные» версии, которые дороже. В то время как, например, автомобильный аккумулятор емкостью 100 А · ч можно купить дешевле 10000 рублей, за аккумулятор глубокого разряда (тягового) 12 В / 100 Ач придется заплатить от 20000.
Что касается наиболее популярных герметичных аккумуляторов AGM, многие из них предназначены в основном для работы в схемах резервного питания в относительно мягких условиях. В документациях к ним можете проверить, подходит ли данный тип также для циклической работы.
Ещё необходимо знать, что отдельные производители предлагают несколько или даже около десятка серий (семейств) гелевых аккумуляторов, которые отличаются, среди прочего, именно способность работать циклично и долговечно.
Где применяются?
Решения позволяют работать с большими пиковыми мощностными нагрузками. Поэтому сфера использования батарей очень обширна. Установка возможна:
- На всех стартерных и ряде тяговых двигателей автомобилей.
- На мототехнике: мопедах, мотоциклах, квадроциклах, скутерах.
- На лодочных моторах.
- На авиационной технике.
- В качестве стартерных чаще используют решения с жидким электролитом, в качестве буферных, а также на сложной технике, включая авиационную, используют, преимущественно решения абсорбированным на сепараторе (по AGM -технологии).
Где используются
Эксплуатационные характеристики и конструктивные особенности позволяют найти широкое применение для свинцово-кислотных аккумуляторных батарей.
К основным сферам использования можно отнести:
- питание систем охраны и сигнализаций;
- применение в качестве источника стартерного тока на автомобиля;
- автономные системы противопожарной безопасности;
- системы аварийного питания в зданиях, отделениях медицинских учреждений;
- кассовые аппараты и электрические весы;
- системы обеспечения бесперебойного питания для компьютеров;
- игрушки;
- лёгкие летательные аппараты и пр.
Конечно же, автомобилистам свинцово-кислотные аккумуляторные батареи известны как источники для подачи стартерного тока. Не зря АКБ называют стартерными.
А вот в качестве тяговых такие батареи используются не так часто, если говорить про питание машин.
Срок службы
Срок службы батареи — это потенциальное время, за которое она будет оставаться в рабочем состоянии и в пределах описанных для неё производителем параметров.За этим сроком на деле стоит максимальный срок работы батареи в типовых условиях функционирования. Снизить срок эксплуатации по неосторожности может ряд факторов. Особенно внимательным нужно быть при пуске. Он должен осуществляться в стабильной среде. Особенно опасны вибрация и скачки температуры.
Недопустимы скачки температуры и во время эксплуатации. Резкое повышение температуры на 10 ° C существенно снизит емкость на 25% и уменьшит срок службы на 50%. Снижение температуры на ту же величину также уменьшит емкость батареи примерно на 25%.
Очень большой вес имеет и соблюдение правил хранения свинцово кислотных аккумуляторов. Помещение должно быть прохладным, сухим.Нельзя осуществлять штабеллирование.
Популярные батареи на жидких электролитах обычно служат 3-4 года, при эксплуатации в стабильной среде и низких нагрузках — возможный срок службы -7-8 лет. Решения, изготовленные по технологи AGM в режиме подзарядки (буферном режиме) способны служить 12-18 лет.
Срок службы никогда не стоит путать с гарантийным, последний всегда — меньше. Например, у изделий, которые способны служить 4 года, гарантийный срок обычно равен 1-2 года.
Разновидности
Опираясь на основные характеристики, актуальные для свинцово-кислотных аккумуляторов, их можно разделить на соответствующие подкатегории.
Для начала стоит акцентировать внимание на возможностях их обслуживания. Тут выделяют такие типы свинцово-кислотных питающих аккумуляторов:
- Обслуживаемые. Предусматривают наличие открытой конструкции. То есть корпус не герметичный. Производитель устанавливает специальные съёмные крышки, позволяющие получить доступ к банкам. Тем самым можно по мере необходимости доливать электролит или кислоту, визуально проверять уровень жидкости и состояние пластин, делать замеры плотности ареометром.
- Необслуживаемые. Корпус полностью герметичный. Обслуживание сводится только к контролю заряда с помощью индикатора, а также подключению АКБ к зарядному устройству.
Популярность вторых вполне очевидна. Обслуживаемые АКБ встречаются всё реже, поскольку технологии совершенствуются, от автомобилистов требуется меньше усилий и внимания для поддержания аккумулятора в рабочем состоянии.
Опираясь на такие основные характеристики как назначение и область применения, выделяют следующие разновидности свинцово-кислотных аккумуляторов.
- Стартерные АКБ. Могут за короткое время выдать большое количество энергии. Из-за этого обладают большим саморазрядом. Необходимые для автомобилей виды батарей. Нуждаются в вентиляции и определённом обслуживании.
- Буферные. Такие виды свинцово-кислотных питающих аккумуляторов служат для того, чтобы в течение небольшого времени хранить сравнительно малый объём энергии. Они функционируют в режиме постоянной подзарядки.
- Для бесперебойных устройств. Чаще всего можно встретить в офисах, предназначаются для компьютерной техники. При возникновении перебоя с электроэнергией позволяют без потери данных успеть завершить работу.
- Для длительного снабжения энергией. Отличаются большим весом и габаритами. Но это позволяет питать потребителей долгое время. Подобные решения можно встретить в медицинской сфере, в отделениях реанимации. Могут питать достаточно внушительное количество потребителей длительное время.
- Гелевые. Существует 2 основных технологии производства гелевых АКБ. Это AGM и GEL. Характеризуются гелеобразным состоянием электролита. Усовершенствованная технология, хотя в её основе всё равно лежат свинец и серная кислота. Гелевые АКБ применяются в автомобилях, используются для работы солнечных батарей и пр.
Чтобы получить определённые характеристики, вносятся соответствующие изменения в конструкцию.
Когда нужно отдать много энергии за короткое время, пластины делают тонкими, но высокими и широкими, уменьшая между ними расстояние. Это позволяет им быстрее отдавать энергию.
Если потребляется мало энергии, но долго, тогда пластины должны быть толстыми, короткими и узкими, расстояние между ними увеличивают.
На параметры АКБ влияют также электролит, применяемые легирующие добавки, такие как кальций, серебро, цинк и пр. Это позволяет выделять ещё несколько разновидностей. Часто встречаются свинцово-кальциевые АКБ.
Зарядка
Автомобильная аккумуляторная батарея сама по себе не может обеспечить авто должным количеством энергии на протяжении длительного времени. Поэтому важно заботиться о пополнении запаса энергии, израсходованной из аккумулятора. Здесь выручает система зарядки. Её задача — производить электрическую энергию, которой снабжаются все потребители электрической энергии транспортного средства во время работы мотора.
Как зарядить свинцово кислотный аккумулятор физически?
Возможны два варианта:
- Постоянным током.
- Переменным током.
Первый вариант проще реализовать физически, но второй вариант более эффективен. Поэтому сначала для зарядки использовался, преимущественно, генератор постоянного тока, а затем на смену ему пришёл генератор переменного или альтернатор. Он и считается наиболее перспективным вариантом зарядки современных транспортных средств.
Необходимость перехода от генератора постоянного тока к альтернатору обусловлена тем, что с ним были трудности при производстве большого количества энергии при низких оборотах мотора.
- Ротор альтернатора обеспечивает вращающееся магнитное поле внутри альтернатора. Обмотки возбуждения ротора принимают электрический ток через щётки.В неподвижной части — статоре производится сама энергия. Специальный вентилятор охлаждения втягивает воздух и создаёт все условия для поддержания нормального температурного режима диодов.
На практике при зарядке, главное, читайте инструкцию производителя. Порядок действий, которые требуется выполнить при зарядке, может отличаться.
Восстановление аккумулятора
Нередко возникает необходимость в восстановлении батареи. Если она сел (часто такое бывает после зимнего «простоя»), главное не паниковать. Как восстановить свинцово кислотный аккумулятор практически? Существует ряд механик восстановления,но наиболее простой и действенный вариант -это многократная зарядка малым током. Главная хитрость: нужно соблюдать перерывы между зарядками. В дело вступает физика. Напряжение возрастает, восприятие к заряду, напротив, уменьшается.. За время паузы электродные потенциалы выходят на один уровень, емкость свинцово кислотного аккумулятора увеличивается, плотность электролита также существенно растёт.
Результат достигнут в тот момент, когда показатели плотности можно считать нормальной для данного типа аккумулятора.
Принцип действия
Принцип работы свинцово кислотного аккумулятора следующий:
- Реагент отрицательной решетки постепенно распадается под действием электролита, образуя ионы свинца. В результате этого распада появляются свободные электроны, которые затем попадают на положительную решетку электрода (через внешнюю цепь);
- Ионы свинца взаимодействуют с электролитом, образуя сульфат свинца. Из-за низкой растворимости он оседает на отрицательной решетке.
- В результате обычный свинец на отрицательной пластине превращается в сернокислый.
- Положительный электрод меньше взаимодействует с электролитом, чем отрицательный. Его основная составляющая – Pb02 реагирует с водой и делится на положительные и отрицательные ионы.
- Положительные передают на пластину соответствующий потенциал, где происходит их слияние с электронами. В ходе реакции восстановления образуется Pb2+, который далее реагирует с электролитом.
- Образовавшийся в результате сернокислый свинец скапливается на положительной решетке, образуя в последствии на ее поверхности свинцовый сульфат.
Батарея получает электроэнергию следующим образом:
- Возле обеих пластин в электролите содержится некоторое количество воды (H+, OH–) и сульфата свинца (Pb2+, SO2/4)
- В процессе зарядки электроны движутся с внешнего источника питания от положительного контакта батареи к отрицательному.
- Поступившие электроны восстанавливают свинец отрицательной пластины.
- Оставшиеся после восстановления свинца ионы и содержащийся в электролите H+ соединяются в H2SO
- На плюсовой пластине приходящий ток выбивает 2 электрона у 2-х валентного свинца, окисляя его до 4-х валентного.
- В результате последующих взаимодействий Pb4+ объединяется с ионами кислорода, восстанавливая материал плюсовой решетки.
- Оставшиеся ионы, реагируя между собой, компенсируют плотность электролита.
Cистематизируем знания, обретаем навыки: дистанционное обучение
Итак, вы познакомились с теорией, касающейся АКБ, классификацией, способами восстановления, зарядкой, но хотите изучить тему глубже, максимально систематизировать знания по этому вопросу, научиться на практике работать с батареей, протестировать свои знания? Отлично!
Вам поможет система онлайн-обучения механиков, электриков и диагностов ELECTUDE. Огромное преимущество онлайн -платформы состоит в том, что она максимально ориентирована на комплексный подход (основы физики + практикоориетированные материалы), и вы сможете получить не просто знания, но и конкретные умения, навыки, а система оценки знаний в виде тестов поможет реально оценить, над какими темами темами еще стоит поработать, в каком темпе двигаться дальше.
Далее мы приводим скриншоты и описания переведённых нами на русский язык модулей, которые непосредственно касаются рассматриваемой выше темы.
Изучайте, присматривайтесь к системе ELECTUDE и находите для себя новый источник не просто для получения знаний, а для пошагового развития практических навыков. Ведь кроме базовых модулей в системе есть специальный виртуальный тренажёр. Он и поможет «прокачаться» по полной. Система отлично подходит для обучения в дистанционном формате, самообучения.
Кислотные аккумуляторы; чтобы больше не было отвратительно читать то что люди о них пишут
Случайно узрел статью с комментариями к ней, и так злость во мне закипела по поводу безграмотности людей в области кислотных (свинцовых в простонародье) аккумуляторов, что не выдержал и решил написать «гикам» (чтобы быть гиком, как оказывается, мало купить дорогой телефон) краткую статью об аккумуляторах. С рассмотрением тех ошибок, которые мне постоянно мусолят глаза и вызывают праведное желание их исправить. Начнем с названия. Я очень часто вижу что тремя буквами А-К-Б называют все что можно зарядить, абсолютно любой аккумулятор. Особенно тремя буквами люди любят называть аккумуляторы типа Li-ion. На самом-же деле АКБ аббревиатура от Аккумуляторная Кислотная Батарея. Под ними подразумевается лишь один тип аккумулятора — свинцовый кислотный. С современной точки зрения это название вызывает некоторый когнитивный диссонанс т.к. на данный момент значение слова «батарейка» т.е. гальванического элемента который зарядить нельзя перешло на слово «батарея». И получается как будто бы из-за слова «аккумуляторная» это аккумулятор который зарядить можно, а из-за слова «батарея» это как будто батарейка которую зарядить нельзя. В реальности-же батарея — просто цепь гальванических элементов и со словом «батарейка» имеет общий лишь корень.
Далее перейдем к некоторым мифам, а именно главный миф — АКБ для автомобиля имеет некие существенные отличия от АКБ для ИБП. И вот нельзя их применять и там и там. С химической точки зрения любые АКБ абсолютно одинаковы
. Как-же они устроены? Очень кратко — если аккумулятор заряжен, то один электрод представляет собой свинцовую решетку с нанесенной на нее пастой из PbO2, второй -такую-же решетку с пастой губчатого свинца. Электролитом служит раствор серной кислоты. В процессе разряда PbO2 восстанавливается и взаимодействуя с серной кислотой образует PbSO4. Свинец на другом электроде окисляется и опять-же образует PbSO4. В конце разрядки мы имеем обе решетчатые пластины заполненные (более или менее) сульфатом свинца. При зарядке аккумулятора происходит электролиз и из сульфата свинца вновь образуется диоксид и металлический свинец. Конечно-же, тут нужно подчеркнуть, что электроды при этом не равны и путать их полярность не стоит т.к. еще на стадии производства в намазку электродов вводятся соответствующие добавки, улучшающие их эксплуатационные свойства. При этом добавки полезные для одного электрода вредны для другого. В очень старые времена, где-то в начале прошлого века, в условиях простых аккумуляторов, вероятно, была допустима переполюсовка аккумулятора по ошибке или с какими-то целями и он какое-то время после этого работал. В том что она допустима сейчас я сомневаюсь.
Таких ячеек в 12В аккумуляторе 6 шт, в 6В — 3 шт. и т.д. Многих вводит в заблуждение значение напряжения на аккумуляторах. Причем значений напряжения номинального, заряда, разряда. С одной стороны, аккумуляторы называются 12В (и 6В, 24В тоже есть, по-моему, даже 4В изредка встречаются) но на корпусе тех-же аккумуляторов для ИБП производитель указывает напряжение выше 13.5В.
Например:
Тут мы видим, что в форсированном режиме напряжение заряда
может быть аж 15В.
Все разъяснит кривая напряжения на АКБ:
Слева мы видим напряжение для аккумулятора из 12 ячеек (24В номинальных), 6 (12В номинальных) и, самое полезное, для одной ячейки. Там-же отмечены области нежелательных напряжений при разряде/ заряде. Из кривой можно сделать выводы:
1 Напряжение 12В, 24В и т.д. являются номинальными и показывают лишь число гальванических ячеек (путем деления на два) в батарее. Это просто название для удобства.
2 Напряжение при заряде могут достигать 2.5 В/ ячейку что для 12В аккумулятора соответствует 15В.
3 Напряжение заряженной батареи считается допустимым при значении 2.1-2.2 В/ячейку, что для 12В аккумулятора соответствует 12.6-13.2В.
Теоретически, батарею можно зарядить и до значений 2.4 В/ячейку или даже немного выше, однако, такая зарядка будет негативно сказываться как на состоянии электродов, так и на концентрации электролита. Однажды, перед сдачей в утиль, я легко зарядил 12В батарею до напряжения ок. 14.5В (уже не помню точное значение).
Итак, автор статьи с которой я начал, решил, что напряжение заряда автомобильной АКБ и АКБ от ИБП отличаются. Это неверно, у них одинаковый тип электродов и одинаковая концентрация серной кислоты в электролите (подобранная давным-давно экспериментальным путем, чтобы предоставлять максимальное напряжение и минимальном саморазряде). Однако, что-же происходит в батарее, почему ее нельзя заряжать при слишком высоком значении напряжения?
Почему в автомобильную АКБ нужно подливать воду, а в АКБ от ИБП не нужно? Эти вопросы позволяют нам плавно перейти в область напряжения разложения воды. Как я написал выше, при зарядке аккумулятора происходит электролиз. Однако, не весь ток расходуется на превращение PbSO4 в PbO2 и Pb. Часть тока будет неизбежно расходоваться и на разложение воды, составляющей значительную часть электролита:
2H2O = 2H2 + O2
Теоретический расчет дает значение напряжения для этой реакции ок. 1.2В. Напоминаю, что напряжение на ячейке при заряде заведомо более 2В. К счастью, активно вода начинает разлагаться только выше 2В, а в промышленности для получения водорода и кислорода из нее процесс ведут и вовсе при 2.1-2.6В (при повышенной температуре). Как бы то ни было, тут мы приходим к выводу, что в конце процесса заряда АКБ будет неизбежно
происходить процесс разложения воды в электролите на элементы. Образующиеся кислород и водород попросту улетучиваются из сферы реакции. Про них бытуют следующие мифы:
1.
Водород крайне взрывоопасен! Перезарядишь аккумулятор и как минимум лишишься комнаты где тот был!
На самом деле, водорода в процессе электролиза выделяется ничтожно мало по сравнению с объемом комнаты. Водород взрывается при концентрации от 4% в воздухе. Если мы допустим, что электролиз ведется в комнате размером 3*3*3 метра или 27 метров куб., то нам понадобится наполнить помещение 27*0.04=1.1 метров куб. водорода. Для получения такого количества H2 нужно было бы полностью разложить ок. 49 моль воды или 884 грамма ее. Если кто-то наблюдал электролиз, то поймет насколько это много. Или попробуем перейти ко времени. При силе тока в стандартной зарядке для крупногабаритных АКБ в 6А, уравнение Фарадея дает время, необходимое для получения этого количества водорода, аж 437 часов или 18.2 дня. Чтобы наполнить комнату водородом до взрывоопасной концентрации нужно забыть про зарядку на 2 с половиной недели! Но даже если это случится, концентрация серной кислоты просто будет расти пока ее раствор не приобретет слишком высокое сопротивление для жалких 12В зарядки и сила тока не станет ничтожной. Да и водород попросту улетучится.
Очень редко случаются взрывы непосредственно в корпусах крупногабаритных АКБ из-за того, что выделяющийся водород по какой-то причине не может покинуть замкнутого пространства. Но и в этом случае нечего страшного не бывает — чаще всего взрыва хватает только на небольшую деформацию верхней части корпуса, но не на разрыв свинцовых соединений. И АКБ еще может работать дальше даже после таких повреждений.
2.
При электролизе может образоваться смертельно ядовитый и, не менее взрывоопасный чем водород, сероводород!
Не наш, периодически попадался миф в англоязычных постах. Теоретически конечно возможно подать такое большое напряжение и создать т.о. такую большую силу тока, что на катоде начнется процесс восстановления сульфат-иона. Напряжение для этого будет достаточным, а продукты восстановления не будут успевать диффундировать подальше от электрода и восстановление будет идти дальше. Но зарядка в пределах десятка-трех вольт и с ограничением силы тока в 6А на такое едва ли способна. Однажды, я наблюдал процесс восстановления сульфата до SO2, да, это возможно; однокурсницы по ошибке что-то сделали не то во время опыта. Но это большая редкость т.к. там концентрация серной кислоты была заметно выше той, что используется в АКБ, была иная конструкция электрода и иной его материал и, естественно, напряжения и сила тока были были непомерными. И SO2 не H2S.
3.
При электролизе мышьяк и сурьма из материала решеток будут восстанавливаться до ядовитых арсина и стибина!
Действительно, решетки содержат относительно много сурьмы, мышьяка в современных решетках, вероятно, нет вообще. При работе АКБ та решетка на которой происходит восстановление, т.е. катод, разрушению не может подвергаться. Выделяйся даже каким-то образом стибин, он бы тут-же взаимодействовал с PbSO4, восстанавливая его до металла.
Однако, некоторая практическая неприятность тут есть. Газообразные водород и кислород могут
увлекать за собой капельки электролита, создавая аэрозоль серной кислоты. Аэрозоль серной кислоты, даже концентрированной, для человека не опасен и просто вызывает кашель. Однако, серная кислота — кошмар для тканей и бумаги. Стоит даже небольшому количеству серной кислоты попасть на одежду и там обязательно появятся дырки или ткань разорвется по этому месту. Через недели, если кислоты много, через месяц, но одежда истлеет.
Так что газовыделения опасаться не стоит с бытовой точки зрения или стоит, но нужно ориентироваться именно на аэрозоль серной кислоты.
Итак, вода начала разлагаться на водород кислород, ее в электролите становится все меньше, что-же дальше? Если это АКБ в котором электролит просто налит в виде слоя жидкости, то начнется повышение саморазряда из-за повышения концентрации серной кислоты. Занятно, что это будет сопровождаться небольшим повышением напряжения (концентрация кислоты растет) на ячейке. Именно поэтому автовладельцы должны постоянно контролировать концентрацию серной кислоты в своих АКБ (при помощи ареометра) и доливать туда воду. Процедура доливания воды — необходимая часть процесса обслуживания
любой АКБ. Кроме одного их типа, и мы сейчас об этом поговорим.
Иметь аккумулятор в котором болтается слой едкой, по отношению к металлам, жидкости конечно-же неудобно, а потому попытки избавиться непосредственно от жидкости предпринимались давно, начались чуть ли не в первой половине 20-го века. К слову сказать, не то чтобы слой серной кислоты прямо плескался вокруг электродов. В реальности она неплохо распределена между электродами и окружающими их сепараторами даже в дешевых моделях. Итак, первым вариантом было использование стекловолокна. Достаточно просто окружить электроды стекловолокном которое пропитано серной кислотой и большинство проблем решится. Этот тип АКБ носит название AGM (absorbent glass mat) и таких АКБ для ИБП подавляющее большинство. Хотя такие АКБ малого форм-фактора и зачастую позиционируются как те, которые можно эксплуатировать в любом положении, с этим нельзя вполне согласиться. Вскрытие крышки стандартного дешевого AGM аккумулятора показывает, что никаких особых крышек там нет, а следовательно, электролит от вытекания удерживают лишь капиллярные силы. Я почти уверен, что если погонять AGM аккумулятор перевернутым вверх дном, то уже после одной зарядки из него польется серная кислота под давление газов.
Второй распространенный тип интереснее, это т.н. гелевые АКБ. А получаются они благодаря следующему. Если подкислять растворимые силикаты, то будет происходить выделение кремневой кислоты:
Na2SiO3 + H2SO4 = Na2SO4 + SiO2
+ H2O
Если исходный раствор силиката не отличается качеством, то кремневая кислота будет выделяться в виде стекловидной массы, но если он достаточно чист, то кремневая кислота осадится в виде красивого куска однородного полупрозрачного геля. На этом и основан способ получения гелевых АКБ — простое добавление силикатов к электролиту вызывает его затвердение в гелеобразную массу. Соответственно, вытекать оттуда уже нечему и АКБ действительно можно эксплуатировать в любом положении. Сам по себе процесс образования геля не повышает емкости АКБ и не улучшает его качеств, однако, производители его используют при производстве наиболее качественных моделей, а потому эти АКБ отличаются высоким качеством и большей емкостью. Занятно, что в обоих случаях носителем электролита является SiO2 в той или иной форме.
Оба типа АКБ объединяются в славный тип VRLA — valve-regulated lead-acid battery который и применяется в ИБП. Формально они считаются необслуживаемыми и терпящими эксплуатацию в любом положении, но это не совсем так. Более того, многие уже встречались с эффектом, когда буквально несколько мл воды возвращают к жизни, казалось бы, дохлую АКБ от ИБП. Так получается, потому что и эти аккумуляторы не капли не застрахованы от электролиза воды в электролите, а следовательно, и пересыхания. Все происходит точно так-же, как в крупногабаритных АКБ. А вот самые дорогие и крутые необслуживаемые АКБ содержат катализатор для рекомбинации выделяющихся газов обратно в воду и вот уже у них корпус действительно выполнен абсолютно герметичным. Обращаю внимание, что по-настоящему герметичным и необслуживаемым может быть и аккумулятор типа AGM и GEL, но они-же могут ими и не быть и не содержать катализатора рекомбинации кислорода и водорода. Тогда, несмотря на казалось бы продвинутую конструкцию, пользователю придется либо чаще покупать новые аккумуляторы, либо доливать воду при помощи шприца.
Хотелось бы добавить несколько слов о режимах разряда. Производители АКБ указывают какой ток максимально допустим для той или иной модели, но нужно понимать, что аккумулятор — просто смесь химических веществ и ЭДС генерируется исключительно химическим путем. Это не конденсатор который, по электрогидравлической аналогии, можно сравнить с неким механическим сосудом (с гибкой мембраной). Хотя АКБ могут выдавать очень большие значения силы тока, в реальности они лучше всего эксплуатируются как раз при небольших токах, что в разряде, что в заряде. Поэтому ИБП, рассчитанные на заряды небольших АКБ, при работе с крупногабаритными будут заряжать их в наиболее щадящем режиме. Впрочем, в течении далеко не одних суток. Интересно обратить внимание на то, что чем выше мощность ИБП, тем больше аккумуляторов последовательно предпочитает собирать производитель. Тут все логично — большие токи разряда маленькие АКБ выдерживают очень плохо.
Подводя итоги:
1. Малогабаритные и крупногабаритные АКБ идентичны по устройству.
2. Для подавляющего большинства АКБ любого размера доливание воды является необходимой частью текущего обслуживания.
3. Лишь немногие из дорогих моделей АКБ содержат механизм рекомбинации газов и могут быть названы действительно необслуживаемыми.
4. Сам по себе водород, который выделяется при заряде (а это равно постоянной работе в ИБП) АКБ, не является существенной угрозой или проблемой.
5. Нужно очень внимательно работать с АКБ, тщательно избегая пролива даже малейших капель электролита, или лишитесь одежды.
6. Разряд и заряд малыми токами являются наиболее предпочтительными режимами эксплуатации АКБ.
Модуль «Свинцово-кислотная аккумуляторная батарея»
В АКБ содержится электрическая энергия, необходимая для запуска грузового транспорта. В грузовике установлены две одинаковые 12-вольтовые батареи, которые соединены последовательно и вместе выдают напряжение равное 24 V (В-вольт). Когда вы поворачиваете ключ зажигания, аккумуляторы подают питание на стартер. Стартер начинает вращать коленчатый вал двигателя. В тот же момент запускается генератор и подзаряжает аккумуляторы.
Аккумуляторные батареи также подают электроэнергию на потребителя, если генератор не обеспечивает достаточную мощность.
На большинстве грузовиках свинцово-кислотные аккумуляторные батареи крепятся к раме , на некоторых – слева, на других–справа. Аккумуляторы могут устанавливаться и под кабиной грузовика.
Эти дополнительные устройства нужны для питания в кабине иных устройств: холодильника, медиаплеера, или зарядного устройства мобильного телефона.
Поскольку устройство содержит опасные кислоты, на его корпус приклеено несколько знаков, указывающих, как с ним безопасно обращаться.
Эти знаки указывают на то, что:
- Устройство следует хранить в труднодоступном месте.
- Есть риск взрыва во время зарядки.
- Аккумулятор следует хранить вдали от открытого огня.
- АКБ содержит опасную едкую кислоту.
- При обслуживании необходимо всегда носить защитные очки.
- Перед началом работы необходимо ознакомиться с руководством по эксплуатации.
- Для утилизации аккумулятор должен быть передан в специальный пункт сбора.
- Никогда не следует выбрасывать аккумулятор вместе с обычным мусором поскольку в нём содержится свинец и кислота.
Каждое устройство содержит информацию о том, с каким типом батареи вы работаете. Эта информация соответствует определённым стандартам.
Существуют различные организации, которые занимаются стандартами, например:
На наклейке указываются необходимые сведения. Например,
- 12 V (вольт): напряжение. Это аккумулятор с напряжением 12 V.
- 230 А/h (ампер-час): ёмкость. Это максимальное количество электрической энергии, которое может выдать аккумулятор при 20 часовом разряде (при конечном напряжении 10, 5 V и температуре 25 ℃). Это максимальное количество электрической энергии, которое может запасти аккумулятор. Данные указываются с учётом времени разряда 20 часов.
- 1200 А, сила тока холодной прокрутки . В соответствии со стандартом DN этот аккумулятор способен обеспечить питание 1200 А в течение 30 секунд с напряжением не ниже 9 V и температурой -18 ℃.
- Две одинаковые аккумуляторные батареи соединены последовательно. Это значит, что вместе они подают напряжение 2×12V=24 V. Емкость аккумулятора постоянна и равна в нашем примере 230 А/h.
- Обе аккумуляторные батареи должны быть одной марки и иметь одинаковую ёмкость и напряжение. Они также должны иметь одинаковую дату производства.
Циклическая и буферная работа АКБ
На некоторых батареях, на корпусе показывается максимальный ток зарядки и два напряжения, или фактически два диапазона напряжений.
Допустимое напряжение цикла использования применяется к циклической работе, то есть когда аккумулятор заряжается в течение нескольких часов, а затем разряжается в течение более длительного или более короткого времени. Примером может служить аккумулятор от электросамоката, работающий циклически.
С другой стороны, режим ожидания – это так называемая буферная работа, когда аккумулятор всегда под напряжением, готов к работе. Типичный пример – ИБП. Еще один пример – резервный источник питания для сигнализации. Тогда аккумулятор постоянно подключен к зарядному устройству – блоку питания, поэтому напряжение ниже, чем в циклическом режиме.
Как показано на фото, напряжение во время плавающего режима должно составлять 13,5 – 13,8 В, в циклическом режиме конечное напряжение заряда может составлять 14,4 – 15,0 В. Поскольку 12-вольтовая батарея имеет шесть ячеек, это дает 2,25 – 2,30 В / ячейку в буферном режиме и 2,4 – 2,5 В / ячейку в циклическом режиме.
Снятие аккумуляторных батарей
Перед тем, как приступить к снятию аккумуляторной батареи с автомобиля, необходимо ознакомиться с руководством по ремонту. Обратите внимание, что инструкция будет отличаться в зависимости от марки АКБ.
- Выньте ключ из замка зажигания.
- Снимите защитный колпачок с кожуха батареи и крышек полюсов (они иногда прикрепляются).
- Сначала отсоедините зажим аккумуляторного кабеля от отрицательной клеммы (если вы сначала отсоедините зажим аккумулятора от плюсовой клеммы, и она случайно соприкоснётся с кузовом, то это вызовет короткое замыкание.
- Затем отсоедините три остальных клеммы аккумуляторной батареи.
- Отсоедините соединительный кабель между аккумуляторами 1 и 2.
- Затем снимите оба крепления.
- Извлеките обе батареи из отсека.
Установка аккумуляторной батареи
Перед тем, как приступить к установке, необходимо ознакомиться с руководством по ремонту. Для каждой марки существует своя инструкция.
- Установите новые аккумуляторы.
- Очистите клеммы и зажимы.
- Установите соединительный кабель с зажимами на отрицательную клемму аккумулятора 2 (задний аккумулятор) и положительную клемму аккумулятора 1 (передний аккумулятор). Обратите особое внимание на клеммы, поскольку вывод «плюс» имеет больший диаметр, чем вывод «минус». Обе клеммы часто сужаются в верхней части.
- Установите зажим для положительной клеммы 2.
- Затем установите зажим для отрицательной клеммы 1.
- Смажьте клеммы и зажимы аккумулятора консистентной смазкой для предотвращения коррозии.
- Наденьте защитные колпачки на крышки полюсов (если они есть).
- Наденьте защитный чехол на корпус аккумуляторной батареи.
- Вставьте ключ в замок зажигания.
Последовательное и параллельное соединение
Под напряжением понимают разность потенциалов между её положительными и отрицательными клеммами. напряжение обозначают буквой U. Единицей напряжения является вольт. Напряжение равно силе тока (А) при определённом сопротивлении(R).
Емкость батареи — это значение максимального количества электрической энергии, которое может содержать батарея. Единицей измерения ёмкости является ампер-час/Ач. Таким образом под мощностью подразумевается ток (А).
Также встречаются комбинированные цепи, в которых батареи соединены как параллельно, так и последовательно. Таким образом увеличивается как ёмкость, так и напряжение.
Разновидности и тестирование
На скриншотах наглядно представлены модули, характеризующие разные типы СКАБ. Это стандартные решения (с жидким электролитом) и устройства, изготовленные по усовершенствованным технологиям.
Прохождение тестов в LMS ELECTUDE позволит разобраться, как вы смогли разобраться в устройстве свинцового аккумулятора, готовы ли вы решить задачи, связанные с ним.